
Pilotstudie zur H₂-Therapie bei der Parkinson-Krankheit:
eine randomisierte, doppelblinde, placebokontrollierte Studie
Asako Yoritaka 1, Masashi Takanashi , Masaaki Hirayama , Toshiki Nakahara , Shigeo Ohta , Nobutaka Hattori
- PMID: 23400965 DOI: 10.1002/mds.25375
Abstrakt
Hintergrund: Oxidativer Stress ist am Fortschreiten der Parkinson-Krankheit (PD) beteiligt. Aktuelle Studien haben bestätigt, dass molekularer Wasserstoff (H₂) in Zellkulturen und Tiermodellen als hochwirksames Antioxidans fungiert. Das Trinken von H₂-gelöstem Wasser (H₂-Wasser) reduzierte den oxidativen Stress und verbesserte die Parkinson-Merkmale bei Modelltieren.
Methoden: In dieser placebokontrollierten, randomisierten, doppelblinden, klinischen Parallelgruppen-Pilotstudie bewerteten die Autoren die Wirksamkeit von H₂-Wasser bei japanischen Patienten mit Levodopa-medikamentierter Parkinson-Krankheit. Die Teilnehmer tranken 48 Wochen lang täglich 1.000 ml H₂-Wasser oder Pseudowasser.
Ergebnisse:
Die UPDRS-Werte (Total Unified Parkinson's Disease Rating Scale) in der H₂-Wasser-Gruppe (n=9) verbesserten sich (Median -1,0; Mittelwert ± Standardabweichung -5,7 ± 8,4), wohingegen die UPDRS-Werte in der Placebogruppe (n =8) verschlechterte sich (Median 4,5; Mittelwert ± Standardabweichung 4,1 ± 9,2). Trotz der minimalen Patientenzahl und der kurzen Studiendauer war der Unterschied signifikant (P < 0,05).
Schlussfolgerungen: Die Ergebnisse zeigten, dass das Trinken von H₂-Wasser sicher und gut verträglich war und eine signifikante Verbesserung der gesamten UPDRS-Werte für Patienten in der H₂-Wasser-Gruppe nachgewiesen wurde.
Therapeutische Inhalation von Wasserstoffgas für Alzheimer-Patienten
und anschließende Langzeitbeobachtung als krankheitsmodifizierende Behandlung:
Eine offene Pilotstudie
von Hirohisa Ono1,*,Yoji Nishijima1 undShigeo Ohta2,*
Abteilungen für Neurochirurgie und Neurologie, Nishijima Hospital, Ohoka, 2835-7, Numazu City 410-0022, Japan
Abteilung für neurologische Medizin, Graduate School of Medicine, Juntendo University, 2-1-1 Hongo, Bunkyo-ku, Tokio 113-8421, Japan
*
Autoren, an die die Korrespondenz gerichtet werden soll.
Arzneimittel 2023 , 16 (3), 434; https://doi.org/10.3390/ph16030434
Eingegangen: 8. Februar 2023 / Überarbeitet: 3. März 2023 / Angenommen: 6. März 2023 / Veröffentlicht: 13. März 2023
(Dieser Artikel gehört zur Sonderausgabe Therapeutisches Potenzial von molekularem Wasserstoff )
Abstrakt
(1) Hintergrund: Die Alzheimer-Krankheit (AD) ist eine fortschreitende und tödliche neurodegenerative Erkrankung. Wasserstoffgas (H 2 ) ist ein therapeutisches medizinisches Gas mit mehreren Funktionen wie Antioxidans, Entzündungshemmer, Zelltod und der Stimulierung des Energiestoffwechsels. Um eine krankheitsmodifizierende Behandlung für AD durch multifaktorielle Mechanismen zu entwickeln, wurde eine offene Pilotstudie zur H2- Behandlung durchgeführt. (2) Methoden: Acht Patienten mit AD inhalierten 6 Monate lang zweimal täglich eine Stunde lang 3 %iges H2 - Gas und folgten dann ein Jahr lang ohne Inhalation von H2Gas. Die Patienten wurden klinisch anhand der kognitiven Subskala der Alzheimer’s Disease Assessment Scale (ADAS-cog) beurteilt. Um die Neuronenintegrität objektiv zu beurteilen, wurde Diffusions-Tensor-Bildgebung (DTI) mit fortgeschrittener Magnetresonanztomographie (MRT) auf Neuronenbündel angewendet, die durch den Hippocampus verlaufen. (3) Ergebnisse: Die mittlere individuelle ADAS-Zahnradveränderung zeigte nach 6 Monaten H2- Behandlung eine signifikante Verbesserung (–4,1) im Vergleich zu unbehandelten Patienten (+2,6). Laut DTI verbesserte die H2 - Behandlung die Integrität der Neuronen, die den Hippocampus passieren, im Vergleich zum Anfangsstadium deutlich. Die Verbesserung durch ADAS-cog- und DTI-Bewertungen blieb während der Nachuntersuchung nach 6 Monaten (signifikant) oder 1 Jahr (nicht signifikant) bestehen. (4) Schlussfolgerungen: Diese Studie legt nahe, dass H2- Behandlung lindert nicht nur vorübergehende Symptome, sondern hat trotz ihrer Einschränkungen auch krankheitsmodifizierende Wirkungen.
Schlüsselwörter: ADAS-Zahnrad ; Alzheimer-Krankheit ; Diffusionstensor-Bildgebung ; neuronale Integrität ; Wasserstoffgas ; krankheitsmodifizierende Behandlung ; mehrere Funktionen
1. Einleitung
Die Alzheimer-Krankheit (AD) ist eine fortschreitende und tödliche neurodegenerative Erkrankung, die zu Beeinträchtigungen der Kognition, des Gedächtnisses und des Verhaltens führt. Bisher konzentrierten sich die meisten AD-Arzneimittelentwicklungen auf die gezielte Bekämpfung eines einzelnen Mechanismus gemäß der herkömmlichen Strategie [ 1 ]. Derzeit zugelassene Medikamente zur AD-Behandlung, darunter Cholinesterasehemmer (Donepezil, Rivastigmin und Galantamin) und ein N-Methyl-D-Asparaginsäure-Rezeptorantagonist (Memantin), sind symptomatisch, verbessern das Fortschreiten der Krankheit jedoch kaum [2 ] . Andererseits ist das Alter der höchste Risikofaktor für AD, was darauf hindeutet, dass mehrere Faktoren auf komplexe Weise an der Ätiologie von AD beteiligt sind [ 3]. In den letzten Jahren wurden multifaktorielle Mechanismen und Multi-Target-Strategien zur Entwicklung krankheitsmodifizierender Medikamente in Betracht gezogen [ 4 , 5 ]. Allerdings kann es schwierig sein, geeignete Kombinationen von zwei oder drei Medikamenten zu finden, da es schwierig ist, auch nur ein einziges wirksames Medikament zu finden. Daher ist es notwendig, den Nutzen eines Moleküls mit mehreren Funktionen als Krankheitsmodifikator zu untersuchen.
Die direkte Ursache der Alzheimer-Krankheit ist das Absterben von Neuronen, und es ist unmöglich, abgestorbene Zellen durch irgendeine Behandlung wiederzubeleben. Zusätzlich zur vorübergehenden Aktivierung ist es jedoch möglich, dass die Integrität überlebender Neuronen nach Beginn der Alzheimer-Krankheit durch eine krankheitsmodifizierende Behandlung verbessert wird [6 ] . Eine idealere Strategie wäre die Wiederherstellung der Integrität überlebender Neuronen mit krankheitsmodifizierenden Therapien, selbst nach Beginn der Alzheimer-Krankheit.
Molekularer Wasserstoff (H 2 ) ist in Abwesenheit eines Katalysators ein inertes Molekül. Lange Zeit wurde angenommen, dass H 2 in Säugetierzellen keine biologische Funktion hat. H 2 wurde erstmals 2007 von einem der Autoren als therapeutisches Antioxidans beschrieben [ 7 ]. Nachfolgende umfangreiche Studien an Modelltieren zeigten, dass H 2 mehrere Funktionen ausübt, wie z. B. Entzündungshemmung, Zelltod und Stimulierung des Energiestoffwechsels, um Wirksamkeit gegen eine Vielzahl von Krankheitsmodellen zu zeigen [ 8 , 9 ]. H 2 hat die Fähigkeit, die Blut-Hirn-Schranke (BBB) durch Gasdiffusion ohne ein spezifisches Arzneimittelabgabesystem zu überwinden [ 7]. Eine Reihe von Tierversuchen legen nahe, dass H 2 das Potenzial hat , neurodegenerative Erkrankungen zu verbessern [ 10 ]. Darüber hinaus haben zahlreiche kleine klinische Studien gezeigt, dass die H 2 -Therapie bei einer Vielzahl von Krankheiten deutlich positive Auswirkungen hat. Bemerkenswert ist, dass in Humanstudien im Zusammenhang mit der Verabreichung einer H2- Therapie keine Nebenwirkungen berichtet wurden [ 11 ]. Tatsächlich wurde die Inhalation von H2-Gas in einer klinischen Phase-I-Studie als sicher bestätigt [ 12 ] .
Mehrere Berichte haben eine deutliche Wirksamkeit von H 2 bei Modelltieren mit Demenz gezeigt [ 13 ]. Darüber hinaus deuten klinische Studien darauf hin, dass H 2 bei Demenz anwendbar ist. Wir haben gezeigt, dass das langfristige Trinken von in H 2 gelöstem Wasser (H 2 -Wasser) die Kognition von Personen mit leichter kognitiver Beeinträchtigung (MCI), die den ApoE4-Genotyp tragen [ 14 ], und die ein hohes Risiko für AD haben [ 15 ], verbessert. Darüber hinaus haben wir kürzlich einen Fallbericht über fortgeschrittene AD veröffentlicht, an dem ein Patient beteiligt war, der durch die kontinuierliche 2-jährige Inhalation von H 2 -Gas eine Verbesserung der Stuhlinkontinenz zeigte [ 16 ]. Also H 2hat ein starkes Potenzial als multifunktionales Mittel zur Verbesserung der Alzheimer-Krankheit.
In der vorliegenden Studie wollten wir eine Behandlung identifizieren, die Neuronen nach Beginn der AD als Krankheitsmodifikator aktiviert. Als objektive Beurteilung der neuronalen Integrität wurde zusätzlich zu einer klinischen Bewertung die Diffusions-Tensor-Bildgebungsmethode (DTI) [ 17 , 18 , 19 ] mit einer fortschrittlichen Magnetresonanztomographietechnik (MRT) angewendet [ 20 ]. Hier vermuten wir, dass die Inhalation von H 2 -Gas eine therapeutische Wirkung hat. Darüber hinaus lässt die Nachbeobachtung im darauffolgenden Jahr ohne Inhalation von H2- Gas darauf schließen, dass diese Behandlung nicht nur vorübergehende Symptome lindert, sondern auch eine krankheitsmodifizierende Wirkung hat.
2. Ergebnisse
2.1. Wasserstoffbehandlung verbesserte AD, wie durch ADAS-cog bewertet
Acht Patienten und ihre Familienangehörigen stimmten der Teilnahme an dieser offenen Studie zu. Tabelle 1 zeigt den Hintergrund der Teilnehmer und Kontrollen ( Tabelle 1 ).
Da die kognitive Subskala der Alzheimer-Krankheitsbewertungsskala (ADAS-cog) weithin als eine der vertrauenswürdigsten Methoden anerkannt ist, haben wir ADAS-cog als klinische Bewertung verwendet [20 ] . Im ADAS-Zahnrad bedeutet ein niedrigerer Wert eine Verbesserung und ein höherer Wert eine Verschlechterung. Das Anfangsstadium des ADAS-Zahnrads der Teilnehmer lag zwischen 19 und 40. Die Patienten inhalierten 6 Monate lang zweimal täglich 1 Stunde lang weiterhin 3 % H 2 -Gas. Während der gesamten Studie wurden keine nachteiligen Auswirkungen festgestellt.
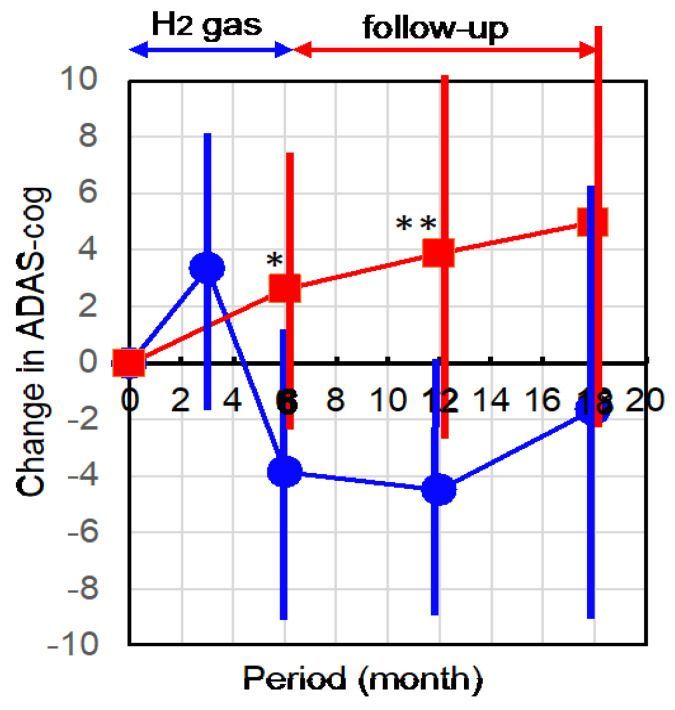
ADAS-Zahnradveränderungen aus jedem Anfangsstadium wurden nach 3 und 6 Monaten und in den Nachbeobachtungszeiträumen für weitere 6 und 12 Monate ermittelt. Die Patienten inhalierten während der Nachbeobachtungszeit kein H 2 -Gas. Abbildung 1 zeigt das zeitabhängige Profil des Mittelwerts jeder Änderung im ADAS-Zahnrad.
Abbildung 1. Änderung des ADAS-Zahnrads im Vergleich zum Anfangsstadium. Die Teilnehmer inhalierten 6 Monate lang zweimal täglich 1 Stunde lang 3 %iges H2-Gas und wurden ein Jahr lang ohne H2-Inhalation nachbeobachtet. ADAS-cog wurde in den ersten drei Monaten (nur H2-Gruppe) und alle sechs Monate bei den Teilnehmern und unbehandelten Kontrollpatienten untersucht, und die Veränderungen gegenüber dem Anfangsstadium wurden mit Standardabweichungen (Fehlerbalken) gemittelt. Blaue Kreise und rote Quadrate zeigen die H2-Gruppe bzw. unbehandelte Kontrollen. * und ** geben Bedeutungen mit p an= 0,017 bzw. 0,004 (H2-Gruppe vs. unbehandelte Kontrollgruppe). Beachten Sie, dass ADAS-cog unabhängig in der Abteilung für Physiotherapie ermittelt wurde, deren Mitarbeiter nicht wussten, ob es sich bei den Probanden um Teilnehmer dieser Studie oder um gewöhnliche ambulante Patienten handelte. Diese Ergebnisse wurden den Ärzten blind über ein elektronisches Diagrammsystem mitgeteilt.
ADAS-cog-Kontrolldaten wurden aus der Datenbank des Nishijima-Krankenhauses bezogen, in der Patienten mit AD mehr als 1,5 Jahre lang etwa alle 6 Monate beobachtet wurden. Der Mittelwert des anfänglichen ADAS-Zahnrads in der unbehandelten Kontrollgruppe betrug 27,8 mit ±3,53 Standardabweichungen, was dem der H 2 -behandelten Gruppe ähnlich war, und das Profil der unbehandelten Gruppe war bei jeder Änderung des ADAS-Zahnrads gleich in guter Übereinstimmung mit früheren Veröffentlichungen [ 21 , 22 ].
Der Mittelwert der ADAS-Zahnradveränderung in der mit H 2 behandelten Gruppe stieg nach den ersten drei Monaten tendenziell an (verschlechterte sich) ( Abbildung 1 ). Die langfristige Verwendung einer Gesichtsmaske kann zu Stress beim Einatmen von H 2 -Gas führen. Nach den nächsten drei Monaten war die ADAS-Zahnradveränderung in der H2- Gruppe im Vergleich zum Anfangsstadium deutlich verringert (verbessert), während sich die unbehandelten Kontrollen kontinuierlich verschlechterten. Die Verbesserung nach den nächsten 3 Monaten (insgesamt 6 Monate) war deutlich größer als bei der unbehandelten Kontrolle ( Abbildung 1 ).
Darüber hinaus machte sich die Verbesserung im Follow-up nach 6 Monaten auch ohne Inhalation von H 2 -Gas bemerkbar, wobei diese Verbesserung im Vergleich zur unbehandelten Gruppe signifikant war ( Abbildung 1 ). Bei der weiteren Nachbeobachtung über weitere 6 Monate setzte sich der Verbesserungstrend fort.
2.2. Verbesserung von Neuronen durch H 2 -Inhalation, beurteilt durch Diffusions-Tensor-Bildgebung
Die Neuronenbündel der weißen Gehirnsubstanz sind stark gerichtet. Die Wasserdiffusionsfähigkeit ist entlang der Richtung des lebenden Bündels viel höher als in anderen Richtungen. Der Unterschied zwischen der Diffusionsfähigkeit entlang und über Bündel hinweg nimmt je nach neuronaler Integrität und axonaler Dichte zu. Neuronenbündel, die an fünf Samenpositionen den gesamten Hippocampus durchquerten, wurden durch dreidimensionale Diagramme visualisiert, und ein zweidimensionales Bild, das den Hippocampus enthielt, wurde in einem Bild angeordnet ( Abbildung 2 ).
Abbildung 2. Anwendung der Diffusionstensor-Bildgebung (DTI) auf die Neuronenbündel, die den gesamten Hippocampus durchlaufen. Für die Auswahl der Neuronenbündel, die den gesamten Hippocampus durchqueren, wurden fünf Saatpunkte gesetzt, wie durch blaue Tore dargestellt. Gelbe Neuronenbündel, die den Hippocampus passieren, wurden mit der DTI-Methode sichtbar gemacht, wie in Materialien und Methoden beschrieben. Es wurden dreidimensionale Bilder von Neuronenbündeln im Gehirn aufgenommen, die durch den Hippocampus verlaufen, und zweidimensionale Bilder, die den Hippocampus enthielten, wurden in einem Bild angeordnet.
Die Werte der fraktionierten Anisotropie (FA) spiegeln die Dichte aktiver Axone innerhalb von Bündeln wider, wobei niedrigere Werte einer geringeren aktiven Axondichte entsprechen. Um die Diffusionsfähigkeit von Wasser entlang der Neuronenbündel als Neuronenintegrität zu bewerten, wurde Diffusion Tensor Imaging (DTI) mit unterschiedlichen FA-Werten bei 0,1 und 0,2 für die gesamte Hippocampusregion durchgeführt [17 , 18 , 19 ] . Die bei FA = 0,2 visualisierte Neuronentraktgröße spiegelt die höhere neuronale Integrität wider, während der visualisierte Neuronentrakt die gesamten Neuronen bei FA = 0,1 widerspiegelt, was weniger empfindlich auf die neuronale Integrität reagiert. Abbildung 2 visualisierte die Neuronenbündel, die an fünf Samenpositionen durch den gesamten Hippocampus gingen ( Abbildung 2 ).
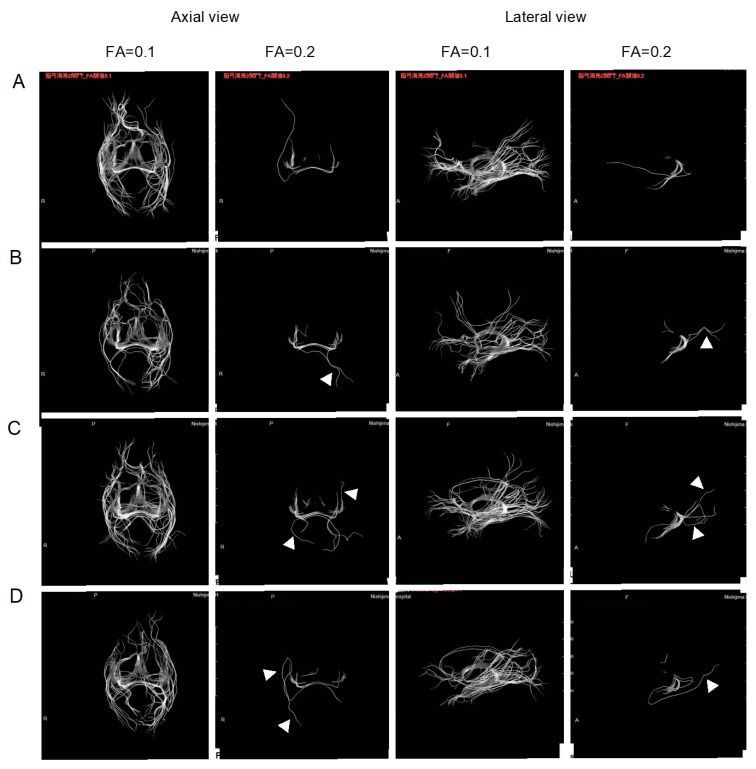
Abbildung 3 zeigt die repräsentativen DTI-Bilder von zwei Patienten, die im Anfangsstadium, 6 Monate nach der Behandlung und in der Nachbeobachtung in den folgenden 6 und 12 Monaten mit seitlicher und axialer Ansicht beobachtet wurden. Die sichtbaren Bündel bei FA = 0,2 waren nach 6-monatiger Behandlung erhöht und blieben während der Nachuntersuchung erhalten. Es ist bemerkenswert, dass sich die sichtbaren Bündel nicht nur in der Größe, sondern auch in der Form veränderten, was darauf hindeutet, dass die H 2 -Behandlung die Integrität des zusätzlichen Bereichs verbesserte, wie durch die Pfeilspitzen in Abbildung 3 dargestellt .
Abbildung 3. Repräsentative Diffusionstensor-Bildgebung (DTI) bei zwei Patienten. Die Patienten inhalierten 6 Monate lang H2-Gas und wurden 12 Monate lang ohne Inhalation von H2-Gas nachbeobachtet. Da die DTI-Veränderungen von Patient zu Patient unterschiedlich sind, werden beispielhaft Bilder von zwei Patienten gezeigt. DTI wurde bei FA = 0,1 und FA = 0,2 in seitlicher und axialer Ansicht sichtbar gemacht. ( A ): Anfangsstadium, ( B ): nach 6-monatiger H2-Inhalation, ( C ): Nachuntersuchung nach den folgenden 6 Monaten und ( D ): Nachuntersuchung nach 12 Monaten. Pfeilspitzen zeigen den Bereich an, dessen Form geändert wurde.
Für eine genauere quantitative Analyse sollten die Werte für jede Messvariation normalisiert werden. Der Wert von FA = 0,1 ist weniger empfindlich für die Neuronenintegrität. Daher wurde der Wert von FA = 0,2 durch den Wert von FA = 0,1 dividiert, der gleichzeitig erhalten wurde, und zur Normalisierung um Abweichungen zwischen den Messungen korrigiert. Daher wurde die Anzahl der Pixel in den entsprechenden Neuronenbündelbahnen bei FA = 0,2 durch die Anzahl der Pixel bei FA = 0,1 normalisiert und der Mittelwert durch Mittelung der 4 Bilder von jedem Patienten aus der rechten und linken Hemisphäre erhalten seitliche und axiale Ansichten. Es wurden fünf AD-Patienten rekrutiert, die der Verwendung ihrer DTI-Daten für diese Studie zugestimmt hatten. Der ADAS-cog-Mittelwert und die Standardabweichungswerte (27,6 ± 6,5) waren denen der H2-Gruppe ähnlich ( Tabelle 1).).
Abbildung 4 zeigt den zeitlichen Verlauf der Mittelwerte mit den Standardfehlern. Der Mittelwert der Neuronenbahnen stieg mit der 6-monatigen H2 - Inhalation im Vergleich zur Kontrolle (*** p = 0,001) und im Vergleich zum Anfangsstadium ( ## p = 0,0036) signifikant an. Nach der 6-monatigen Nachuntersuchung blieb die Verbesserung im Vergleich zum Anfangsstadium signifikant bestehen ( # p = 0,011). Darüber hinaus war der Mittelwert nach 12-monatigem Follow-up höher als der Ausgangswert, obwohl keine Signifikanz bestand.
Abbildung 4. Quantitative Analysen des zeitlichen Verlaufs der Diffusionstensor-Bildgebung (DTI). Die Teilnehmer inhalierten 6 Monate lang H2-Gas und wurden 12 Monate lang ohne Inhalation von H2-Gas nachbeobachtet. DTI wurde zu den angegebenen Zeiten für Teilnehmer und unbehandelte Kontrollpatienten untersucht. Die Pixelzahlen der entsprechenden neuronalen Bündelbahnen in FA = 0,1 und FA = 0,2 wurden für die rechte und linke Hemisphäre mit seitlicher und axialer Ansicht ermittelt. Jeder Wert in FA = 0,2 wurde durch den in FA = 0,1 dividiert und diese normalisierten Werte von Patienten mit 4 Bildern wurden mit den Standardfehlern (Fehlerbalken) gemittelt. Blaue Kreise und rote Quadrate zeigen die H2-Gruppe bzw. unbehandelte Kontrollen. *** gibt Bedeutung mit p an= 0,001 vs. unbehandelte Gruppe. ## und # in der H2-Gruppe geben Signifikanzen mit p = 0,0036 bzw. p = 0,011 im Vergleich zum Anfangsstadium der H2-Gruppe an. # in der unbehandelten Kontrollgruppe zeigt eine Signifikanz mit p = 0,024 gegenüber dem Anfangsstadium der Kontrollgruppe an.
Insgesamt verbesserte die Inhalation von H 2 -Gas über 6 Monate die Alzheimer-Krankheit, wie anhand des klinischen ADAS-Zahnrads und des objektiven DTI ermittelt wurde. Darüber hinaus hielt die Verbesserung zumindest nach 6 Monaten ohne H2- Behandlung an, was darauf hindeutet, dass diese Behandlung nicht nur eine vorübergehende Linderung, sondern auch eine krankheitsmodifizierende Wirkung bringt.
3. Diskussion
Es ist allgemein anerkannt, dass die Anreicherung des Amyloid-β-Proteins den neuronalen Tod bei AD induziert [ 23 ]. Alternativ spielt oxidativer Stress eine wichtige Rolle bei AD und gilt als einer der zentralen Faktoren in der Pathogenese von AD [ 24 ]. Da oxidativer Stress die Expression zahlreicher Gene beeinflusst, die viele pathologische Phänomene wie erhöhte Amyloidproduktion, Modifikation des Tau-Proteins, Autophagie und Apoptose regulieren, könnte die antioxidative Wirkung von H 2 seine wichtigste neuroprotektive Eigenschaft sein [ 11 ] .
Die Pathogenese von AD beinhaltet starke Wechselwirkungen mit immunologischen Mechanismen im Gehirn [ 25 ]. Entzündungen treten offenbar in pathologisch gefährdeten Regionen des AD-Gehirns auf [ 26 ].
Darüber hinaus wurde die Herunterregulierung des Energiestoffwechsels als eines der Risiken und/oder Ursachen von AD angesehen. Defizite bei der Glukoseverfügbarkeit und der Mitochondrienfunktion sind bekannte Kennzeichen der Gehirnalterung und treten besonders bei neurodegenerativen Erkrankungen wie AD hervor [ 27 ], was darauf hindeutet, dass der Energiestoffwechsel an ihrem Fortschreiten beteiligt ist. Tatsächlich wurde vorgeschlagen, dass mäßige Bewegung dazu beitragen kann, das Fortschreiten der Alzheimer-Krankheit zu verzögern [ 28 ].
Daher besteht eine Strategie für die AD-Therapie oder Arzneimittelentwicklung darin, oxidativen Stress, Entzündungen und Energiestoffwechsel zu modulieren [ 29 ].
In jüngster Zeit wurden eine Reihe randomisierter klinischer Studien mit der Inhalation von H 2 -Gas bei verschiedenen Krankheiten durchgeführt. Beispielsweise verbesserte die H2 - Inhalation die körperliche und respiratorische Funktion bei akuten Post-COVID-19-Patienten [ 30 ]; ein Atemnot-, Husten- und Sputum-Skalen-Score bei Patienten mit akuter Verschlimmerung einer chronisch obstruktiven Lungenerkrankung [ 31 ]; Funktionszustand der roten Blutkörperchen, der mit einem günstigeren Verlauf der frühen postoperativen Phase einhergeht [ 32 ]; und verbesserte systemische Entzündung und Leberhistologie bei Patienten mit mittelschwerer bis schwerer nichtalkoholischer Fettlebererkrankung [ 33 ].
Als molekularer Mechanismus, durch den H 2 mehrere Funktionen ausübt, wurde kürzlich ein Zielmolekül von H 2 identifiziert [ 34 ]. Eine oxidierte Form von Porphyrin katalysiert die Reaktion von H 2 mit Hydroxylradikalen, den oxidativsten freien Radikalen, um den oxidativen Stress zu reduzieren. Darüber hinaus aktiviert H 2 als sekundäre antioxidative Funktion den NF-E2-bezogenen Faktor 2 (Nrf2) [ 9 ], der oxidativen Stress durch die Expression einer Vielzahl antioxidativer Enzyme reduziert [ 35 ].
Darüber hinaus hat H 2 eine Anti-Zelltod-Funktion, indem es die Ferroptose durch eine Verringerung des Peroxids hemmt [ 36 ] und Pro- bzw. Anti-Tod-Faktoren herunter- bzw. hochreguliert [ 37 ].
H 2 lindert Entzündungen, indem es proinflammatorische Zytokine verringert [ 38 ]. H 2 modifiziert den Phospholipid-Mediator, der die Ca 2+ -Signalisierung hemmt , was zur Unterdrückung des Transkriptionswegs des Kernfaktors aktivierter T-Zellen (NFAT) führt, um proinflammatorische Zytokine herunterzuregulieren [ 8 , 36 ]. Die NFAT-Signalübertragung spielt eine wichtige Rolle bei der Förderung der Amyloid-β-vermittelten Neurodegeneration und beeinflusst AD [ 39 ]. Darüber hinaus ist der NFAT-Transkriptionsweg an der Amyloid-β-Synaptotoxizität beteiligt [ 40 ]. Daher könnte die Unterdrückung der NFAT-Transkriptionsregulation die vorteilhaften Wirkungen von H 2 auf die AD-Verbesserung erklären.
H 2 hemmt die Kettenreaktion freier Radikale, was zu einer Verringerung der Fettsäureperoxidation und ihrer Endprodukte wie 4-Hydroxy-Nonenal (4-HNE) führt, das bekanntermaßen als Überträger verschiedener Arten zellulärer Signalübertragung dient. Die Abnahme von 4-HNE wiederum fördert die Expression von PGC-1α, gefolgt von einer Erhöhung von FGF21, einem Schlüsselregulator des Energiestoffwechsels, und mehreren Enzymen, die mit der β-Oxidation zusammenhängen [ 41 , 42 ].
Die Abgabe von Arzneimitteln an das Gehirn, die die Blut-Hirn-Schranke passieren können, ist eines der schwerwiegenden Probleme bei der Entwicklung von Therapeutika für AD. H 2 ist unpolar, nichtionisch und klein, sodass es die Blut-Hirn-Schranke passieren und durch schnelle Diffusion leicht Neuronen erreichen kann [ 7 ].
Angesichts der vielfältigen Risiken und/oder Ursachen für die Ätiologie der Alzheimer-Krankheit wird davon ausgegangen, dass H 2 mit diesen vielfältigen Funktionen ein deutliches Potenzial zur Verbesserung der Alzheimer-Krankheit aufweist.
In der vorliegenden Studie haben wir gezeigt, dass die H2 - Behandlung zu einer deutlichen Verbesserung führte, wenn die Wirkungen mit denen von Donepezil verglichen wurden: Die Verabreichung von Donepezil verringerte (ein niedrigerer Wert bedeutete Verbesserung) den ADAS-cog um −2,9 oder −3,1 Punkte nach 24 Wochen [ 43 , 44 ]; jedoch kehrten die Werte nach 6 Monaten trotz kontinuierlicher Verabreichung wieder auf das Ausgangsniveau zurück [ 21 ]. Andererseits betrug in der vorliegenden Studie der Mittelwert der ADAS-Zahnradveränderung –4,1 Punkte gegenüber dem Anfangsstadium nach der 6-monatigen Behandlung mit H 2 . Diese Veränderung durch H 2 kann im Vergleich zu zugelassenen Wirkstoffen wie Donepezil deutlich sein. In dieser Folgestudie blieb der mittlere ADAS-cog in der mit H 2 behandelten Gruppe nach 6 Monaten deutlich besser als in der unbehandelten Kontrollgruppe, und die Wirkung hielt tendenziell 1 Jahr lang an. Darüber hinaus zeigte diese Nachuntersuchung bei DTI auch, dass die neuronale Integrität nach 6-monatiger Behandlung deutlich höher war als im Anfangsstadium. Darüber hinaus hielt der DTI-Verbesserungseffekt tendenziell ein Jahr lang an. Diese Ergebnisse legen nahe, dass eine sechsmonatige H2 - Inhalation die krankheitsmodifizierenden Wirkungen für mindestens sechs Monate aufrechterhielt.
Abschließend weisen wir auf die Einschränkungen dieser Studie hin. An dieser Studie war eine kleine Anzahl nicht randomisierter Patienten beteiligt. Weitere Studien erfordern eine placebokontrollierte Doppelblindstudie, um die Wirkung bei einer großen Anzahl von Patienten zu klären. Trotz dieser Einschränkungen legt diese Studie nahe, dass die Inhalation von H2 - Gas das Potenzial hat, nicht nur vorübergehende Linderung, sondern auch krankheitsmodifizierende Wirkungen zu bewirken.
4. Materialien und Methoden
4.1. Genehmigung für diese Studie
Diese Studie wurde in Übereinstimmung mit dem „Ethikkodex des Weltärztebundes (Erklärung von Helsinki)“ durchgeführt. Das Protokoll dieser klinischen Studie wurde von der Ethikkommission des Nishijima-Krankenhauses genehmigt und unter der URL http://www.jmacct.med.or.jp vorregistriert . Registrierung klinischer Studien – JMACCT-ID: JMA-IIA00308. Für alle Patienten erhielten wir eine schriftliche Einverständniserklärung eines Familienmitglieds.
4.2. Patientenauswahl
Die Kriterien für die Einbeziehung von AD-Patienten waren wie folgt: (1) Diagnose von AD gemäß den Empfehlungen der National Institute on Aging-Alzheimer's Association Group (NIA/AA) [ 45 ] ; (2) ein ADAS-Cog-Score von mehr als 10 oder weniger als 50 oder ein entsprechender Score, der aus dem Mini-Mental-State-Examen (MMSE) unter Verwendung der Formel 70-(MMSE x 2,33) [46] umgerechnet wurde]; (3) Eine Behandlung mit mindestens einem der Anti-Cholinesterase-Medikamente und/oder einem NMDA-Rezeptor-Antagonisten wurde bereits versucht und dennoch verschlechterten sich die ADAS-Werte. (4) Routinebehandlung in der Klinik für neurologische Demenz mit mehreren ADAS-cog/MMSE-Tests alle 6 Monate bei jüngster Verschlechterung; (5) keine signifikante Atemwegserkrankung wie chronisch obstruktive Lungenerkrankung (COPD), Lungenentzündung, Bronchitis oder Asthma, die eine ausreichende H 2 -Inhalation beeinträchtigen könnte ; und (6) Erfahrung mit der MRT des Gehirns. Die Patienten erhielten weiterhin mindestens eines der folgenden Arzneimittel: Donepezil, Galantamin, Rivastigmin oder Memantin.
Den Patienten, die diese Einschlusskriterien erfüllten, wurde eine einwöchige Testinhalation und Testmedikation angeboten. Es wurde bestätigt, dass die Patienten bei einem Blutspiegel von weniger als 0,8 mÄq/dL keine Symptome zeigten und keine Nieren- oder Leberfunktionsstörungen zeigten. Die Familien/Pflegekräfte der Patienten kümmerten sich um den H2-Generator, einschließlich der Überprüfung des Wasserstands des Generators Lassen Sie die Patienten 1 Stunde lang H 2 -Gas einatmen .
4.3. Sammlung von Daten von unbehandelten Kontrollpatienten
Als unbehandelte Kontrollen für die ADAS-Zahnradbewertung erfüllten 19 Patienten mit AD von 94 Patienten in der Datenbank des Nishijima-Krankenhauses die folgenden Kriterien: Das anfängliche ADS-Zahnrad lag im Bereich von 19 bis 40 und die Daten des ADAS-Zahnrads wurden alle 6 Monate über einen Zeitraum von mehr als 1,5 Jahren im Nishijima-Krankenhaus beobachtet. Die mittleren und Standardabweichungswerte des ADS-cog der 19 Patienten betrugen im anfänglichen ADAS-cog 27,8 ± 3,5, was denen der H2-Gruppe ähnlich ist ( Tabelle 1 ).
Als unbehandelte Kontrollgruppe für DTI stimmten 5 Patienten der Verwendung ihrer DTI-Daten für diese Studie zu. Die mittleren ADAS-Cog- und Standardabweichungswerte betrugen 27,6 ± 6,5, was denen der H2-Gruppe ähnlich ist ( Tabelle 1 ).
4.4. Behandlung
Die Patienten inhalierten 1 Stunde lang zweimal täglich 3 % H 2 über eine normale Gesichtsmaske zu Hause oder in einem Pflegeheim. Die Familienangehörigen beobachteten die Patienten stets, um eine kontinuierliche Inhalation über eine Stunde mit der Gesichtsmaske sicherzustellen. H 2 -Gas (3 %) mit 21 % Sauerstoff wurde mit einem tragbaren H 2 -Generator (Nishijima/Enoa-Wasserstoffgasgenerator) wie zuvor beschrieben erzeugt [ 47 ]. Der H 2 -Generator wurde jeden Monat auf ausreichende Gasproduktion überprüft.
4.5. ADAS-Zahnraduntersuchung
Da die kognitive Subskala der Alzheimer-Krankheitsbewertungsskala (ADAS-cog) weithin als eine der vertrauenswürdigsten Methoden anerkannt ist, haben wir ADAS-cog als klinische Bewertung verwendet [20 ] . Im ADAS-Zahnrad bedeutet ein niedrigerer Wert eine Verbesserung und ein höherer Wert eine Verschlechterung. Das ADAS-Cog besteht aus 11 Fragen: Worterinnerungsaufgabe, Benennen von Objekten und Fingern, Befolgen von Befehlen, Konstruktionspraxis, Ideenpraxis, Orientierung, Worterkennungsaufgabe, Merken von Testrichtungen, gesprochene Sprache, Verständnis und Wortfindungsschwierigkeiten.
Die klinische Wirksamkeit wurde durch Überwachung des ADAS-Zahnrads bewertet [ 20 ]. ADAS-cog wurde unabhängig in der Abteilung für Physiotherapie ermittelt, deren Mitarbeiter nicht wussten, ob es sich bei den Probanden um Teilnehmer dieser Studie oder um gewöhnliche ambulante Patienten handelte. Diese Ergebnisse wurden den Ärzten blind über ein elektronisches Diagrammsystem mitgeteilt.
4.6. Messung der Integrität von Neuronen durch Diffusionstensor-Bildgebung
Die Neuronenbündel der weißen Gehirnsubstanz sind stark gerichtet. Die Wasserdiffusionsfähigkeit ist entlang der Richtung des lebenden Bündels viel höher als in anderen Richtungen. Der Unterschied zwischen der Diffusionsfähigkeit entlang und über Bündel hinweg nimmt je nach neuronaler Integrität und axonaler Dichte zu. Die Werte der fraktionierten Anisotropie (FA) spiegeln die Dichte aktiver Axone innerhalb von Bündeln wider, wobei niedrigere Werte einer geringeren aktiven Axondichte entsprechen. Um die Diffusionsfähigkeit von Wasser entlang der Neuronenbündel als Neuronenintegrität zu bewerten, wurde Diffusion Tensor Imaging (DTI) mit unterschiedlichen FA-Werten bei 0,1 und 0,2 für die gesamte Hippocampusregion durchgeführt [17 , 18 , 19 ] .
Zur objektiven Beurteilung wurde in der radiologischen Abteilung ein Gehirn-MRT untersucht. An den volumetrischen Messstellen, an denen die Neuronenbündel durch den gesamten Hippocampus liefen, wurden fünf Saatpunkte gesetzt ( Abbildung 2 ). Die digitale Traktographie-Bildgebung wurde mit Neuro3D mit der GRAPPA-Technik durchgeführt. DTI wurde mit FA-Werten von 0,1 und 0,2 erhalten. Die Traktgröße wurde aus der Pixelzahl der Traktbilder berechnet, und die Anzahl der Pixel im Trakt wurde mit der ImageJ-Software berechnet.
Die Mitarbeiter dieser Abteilungen meldeten die Ergebnisse blind über ein elektronisches Diagrammsystem an die Ärzte. Sie hatten keine Informationen darüber, ob es sich bei den Probanden um Studienteilnehmer oder gewöhnliche ambulante Patienten handelte.
4.7. Statistische Analyse
Die statistische Analyse wurde von einem akademischen Biostatistiker unter Verwendung der SAS-Software Version 9.2 (SAS Institute Inc., Cary, NC, USA) anhand des Student- t -Tests mit zwei Enden durchgeführt. p < 0,05 gilt als signifikant.
5. Schlussfolgerungen
Diese Studie legt nahe, dass die H2 - Inhalation laut ADAS-cog und DTI zu deutlichen Verbesserungen führte und, was noch wichtiger ist, nicht nur eine vorübergehende Linderung bewirkte, sondern auch die Wirkung ohne H2-Behandlung für mindestens 6 Monate aufrechterhielt . Allerdings umfasste diese Studie zur H2 - Inhalation bei AD-Patienten eine kleine Anzahl von Patienten und war eine offene klinische Studie. Weitere Studien erfordern eine randomisierte, placebokontrollierte Gruppe, um die Wirkung bei einer großen Anzahl von Patienten zu klären. Trotz dieser Einschränkungen schlagen wir vor, dass die H2 - Inhalation ein Kandidat für die krankheitsmodifizierende Behandlung von AD ist, da die Wirkung der H2-Inhalation auffällig ist.
https://pubmed.ncbi.nlm.nih.gov/36986533/




Hue Light Europa
Orsoyer Str. 6
47495 Rheinberg
Inhaber: DrHydrogens Wasserstoff-Therapie UG (haftungebeschränkt)
© 2023 Huelight Europa -
Disclaimer:
Alle hier getätigten Aussagen entsprechen entweder dem gesicherten Stand wissenschaftlicher Erkenntnis (OLG Hamburg, Urt. v. 16.12.2010, Az: 3 U 161/09), oder dienen rein der Information. Auf jeden Fall soll nicht der Eindruck erweckt werden, dass dort Versprechungen auf eine Heilung damit verbunden ist. Die Nutzung unserer auf Selbstheilung ausgericheteten Systeme ersetzen nicht den Besuch beim Arzt oder Heilpraktiker. Bei Erkrankungen wenden Sie sich bitte zuerst an Ihren Arzt oder Heilpraktiker

